留学中の小池佑佳 先生の論文がNatureに掲載されました
筋萎縮性側索硬化症/前頭側頭型認知症(ALS/FTD)の発症リスクである,UNC13A遺伝子の変異と,TDP-43蛋白の機能障害をつなぐ分子メカニズムを小池佑佳 先生が留学先のMayo Clinic Floridaで明らかにしました.以下論文の紹介になります.
これは,Stanford大学Aaron Gitler 教授のチームとMayo Clinic Floridaの共同プロジェクトであり,Leonard Petrucelli 教授,Mercedes Prudencio 博士のご指導の下,研究に取り組み,研究成果を共同筆頭著者として発表しました.本論文は,英国科学雑誌「Nature」に2022年2月23 日 (現地時間) に公開されました.
研究成果のポイント:
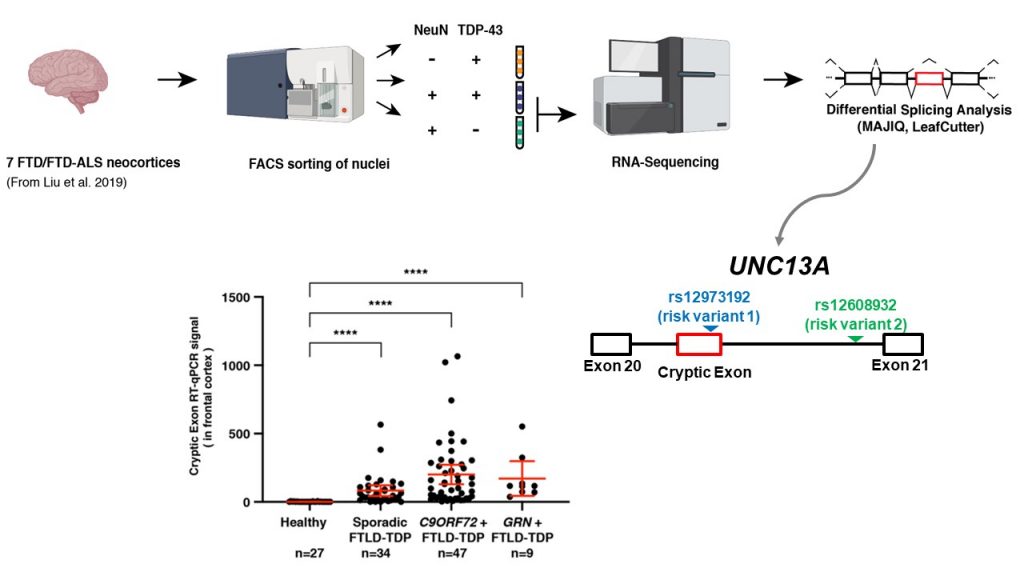
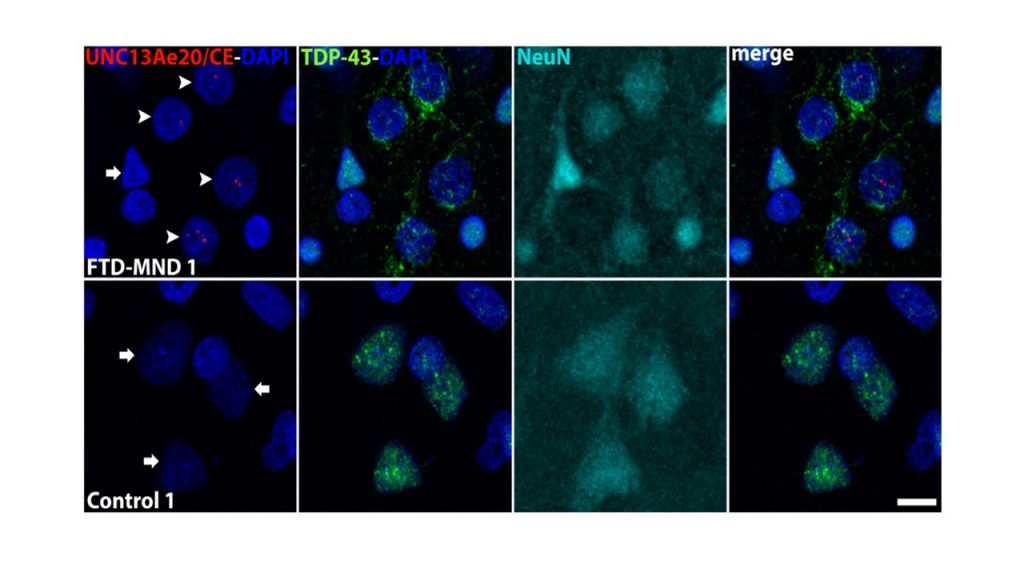
ALS/FTDの原因タンパク質であるTDP-43は,「スプライシング」と呼ばれるRNAの編集機構を介して,様々な遺伝子の発現調節 (遺伝子の設計図であるDNAから,RNAを介して,タンパク質を適切に合成させるメカニズム) に関わっています.本研究では,まず,ALS/FTD患者さんの脳で,UNC13Aという遺伝子に異常なスプライシングが生じていることを見出しました.そして,TDP-43タンパク質の量を低下させると,UNC13A遺伝子の異常なスプライシングが増加し,正常なUNC13A蛋白質は減少することを,神経系の細胞で明らかにしました.このUNC13A遺伝子の変異(一塩基多型)は,以前からALS/FTDの重要なリスク因子として知られていました.しかし,この変異がどのように疾患リスクの上昇に繋がるのか,これまでは明らかになっていませんでした.今回,このUNC13A遺伝子の変異が,TDP-43による正常なスプライシングの調節を障害すること,そして,TDP-43の機能が低下すると,UNC13A遺伝子の異常なスプライシングがさらに増加することを示しました。今回の研究成果は,UNC13A遺伝子の変異とALS/FTDの発症リスクを直接結ぶ分子メカニズムを説明するものであり,さらに,この「異常なスプライシング」を検出することは,将来的に,診療の場で,有効な診断ツールとなる可能性を秘めています.
最後に,当科では,長年,TDP-43蛋白のRNA代謝に関する機能を,様々なアプローチで研究しています.その研究室で学ぶ者の一人として,留学先で,関連性のある本研究に取り組めたことは,とても幸運に思います.同時に,留学にあたり,素地となる部分のご指導を頂きました,小野寺理 教授と分子神経疾患解析学分野の諸先輩方に,改めて感謝致します.